- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体可通过流式、WB(检测指标有CD9,CD63,CD81)、电镜观察、NTA粒径追踪等手段检测,普遍应用于药物载体、疾病诊断marker、精细医疗、一些病症治病等方面研究。由于外泌体直径小,样本含量低,提取十分困难。已有的外泌体分离方式有密度梯度离心、超滤离心法、免疫磁珠抗体捕获、商用试剂盒等。但到目前为止,仍没有一种提取方法能同时保证外泌体的含量、纯度以及生物活性。外泌体是细胞间进行物质运输和信息交流的重要工具,可以通过调节免疫功能促进一些病症的增殖,血管新生和一些病症转移。与细菌传染,帮助细菌逃避免疫关系很大,并与心血管疾病,老年痴呆等疾病具有密切关系外泌体的提取、分离方法:免疫亲和层析法。芜湖外泌体提取试剂进货价

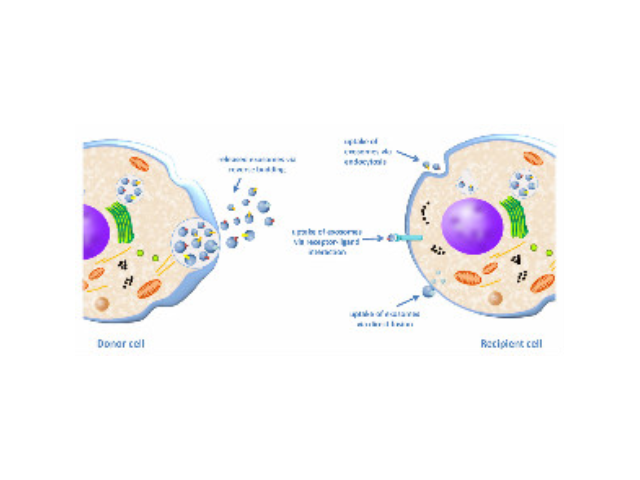
人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。三是外泌体膜可以与靶细胞膜直接融合,非选择性的释放其所含的蛋白质、mRNA以及microRNA广州外泌体提取试剂直销价外泌体表面有其特异性标记物,用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合。
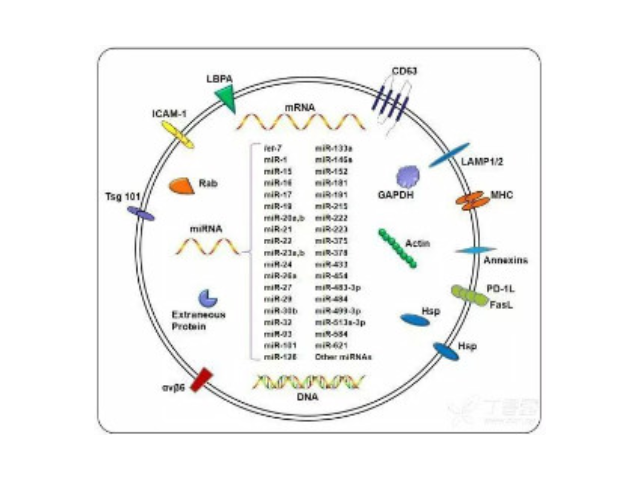
1996年GRaposo等发现类似于B淋巴细胞的免疫细胞也会分泌抗原呈递外泌体(antigenpresentingvesicle),所分泌的外泌体可以直接刺激效应CD4+细胞的抗一些病症反应。2007年HValadi等进一步发现细胞之间可以通过外泌体中RNA交换遗传物质。随着有关外泌体研究越来越多,研究者发现它普遍参与了机体免疫应答、抗原呈递、细胞分化、一些病症生长于侵袭等各种生物过程中。目前的主流观点认为,外泌体的产生过程为:细胞膜内陷,形成内体(endosome),再形成多泡体(multivesicularbodies,MVB),较后分泌到胞外成为外泌体。外泌体中携带有母细胞的多种蛋白质、脂类、DNA和RNA等重要信息。外泌体较早见于1981年,EGTrams等在体外培养的绵羊红细胞上清液中发现了有膜结构的小囊泡,并命名为exosome。对于外泌体的作用,当时推测为细胞排泄废物的一种方式。
在这项新的研究中,经过基因修饰的外泌体(被称作iExosome)能够运送特异性地靶向KRAS突变基因的小RNA分子,从而导致胰腺病模式小鼠病情缓解,增加它们的总存活率。这些研究人员采用了一种被称作RNA干扰(RNAi)的靶向方法:利用这些天然的纳米颗粒(即外泌体)运送小干扰RNA(siRNA)或短发夹RNA(shRNA)分子来靶向胰腺病细胞中的KRAS突变基因,从而影响多种胰腺病模型的一些病症负荷和存活。他们证实外泌体能够作为一种高效的RNAi载体发挥作用,这是因为这些纳米大小的囊泡(即外泌体)轻松地在体内迁移和进入靶细胞(包括病细胞)中。外泌体提取:回收率不稳定(可能与转子类型有关),纯度也受到质疑。

外泌体(exosomes)是活细胞经过"内吞-融合-外排"等一系列调控过程而形成的膜性囊泡,来源于晚期核内体(也称为多囊泡体),直径约为30-150nm,密度在1.13-1.21g/ml,天然存在于血液、唾液、尿液及母乳等体液中,同时外泌体也存在于组织和细胞间隙中。人体中几乎所有类型的细胞均能产生外泌体,人体中大约有1014个外泌体,大约平均每个细胞产生1000-10000个。外泌体中含有核酸(DNA、miRNA、lncRNA、mRNA、tRF等)、蛋白和脂类,在细胞间物质和信息转导中发挥重要作用,研究表明其在干细胞、免疫调控、瘤转移、血管生成以及生物标志物等领域都发挥着不可替代的作用外泌体提取:超滤膜也可用于分离外泌体。无锡外泌体提取试剂哪家便宜
可以使用NanoSight®或电子显微镜分析纯化的外泌体,以评估近似外泌体大小范围和浓度。芜湖外泌体提取试剂进货价
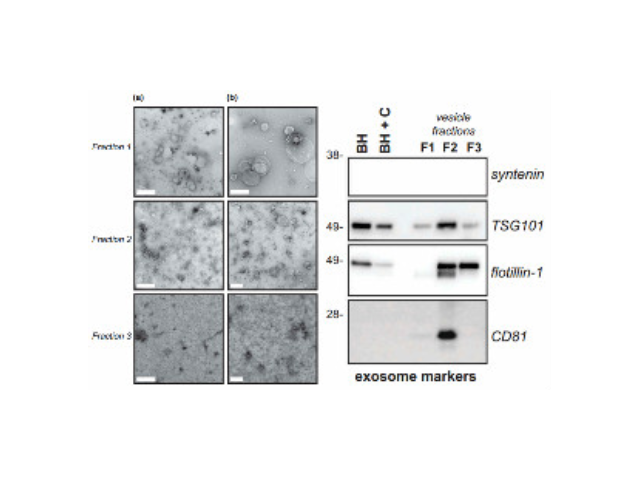
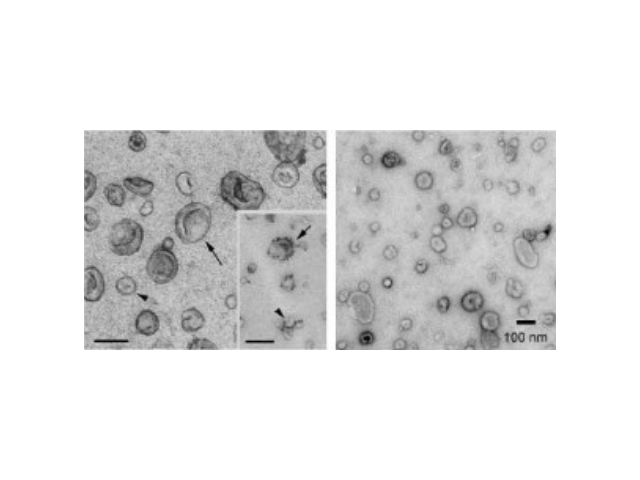
外泌体鉴定:外泌体分离之后,需要经过一系列鉴定才能确定分离的是外泌体。鉴定方法从物理特征到表面分子标志物,多角度进行鉴定。l透射电镜鉴定法:简称TEM,适合外泌体双层囊膜超微结构观察,即通常为茶托型或一侧凹陷的半球形。l纳米颗粒追踪分析法:简称NTA,该方法能保证外泌体原始状态、检测速度快,检测后能提供外泌体粒径和浓度信息。lWesternblot分子标志物检测:外泌体标志蛋白包括四跨膜蛋白家族,如CD9、CD63和CD81;细胞质蛋白,如肌动蛋白(Actin)和钙磷脂结合蛋白(Annexins);使用可截留100KD分子量的膜,通过离心截留上清中的外泌体,截留完成后芜湖外泌体提取试剂进货价
外泌体(exosome),特指直径在40-100nm的盘状囊泡。其主要来源于细胞内内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。现已证实可以分泌外泌体的细胞有:肥大细胞、淋巴细胞、树突状细胞、瘤细胞、间充质干细胞等。外泌体在免疫中抗原呈递、瘤的生长与迁移、组织损伤的修复等生理病理上起着重要的作用。同时,不同细胞分泌的外泌体具有不用的组成成分和功能,可作为疾病诊断的生物标志物。细胞外囊泡是蛋白质、mRNA、miRNA和脂质运输来完成细胞间通讯通路的重要媒介,根据它们的大小和发生分为三类,包括外泌体、微泡和凋亡小体。其中,外泌体是直径大约为40-100nm的包装囊泡...
- 南京外泌体提取试剂厂家推荐 2024-11-13
- 外泌体提取试剂厂家现货 2024-11-13
- 南昌外泌体提取试剂销售厂家 2024-11-13
- 郑州正规外泌体提取试剂推荐厂家 2024-11-13
- 长沙正规外泌体提取试剂单价 2024-11-13
- 贵阳外泌体提取试剂报价 2024-11-13
- 昆明外泌体提取试剂哪家便宜 2024-11-12
- 郑州正规外泌体提取试剂厂家供应 2024-11-11
- 成都正规外泌体提取试剂厂家 2024-11-11
- 昆明外泌体提取试剂供应商 2024-11-11
- 天津外泌体提取试剂产品介绍 2024-11-11
- 深圳外泌体提取试剂平均价格 2024-11-11
- 厦门正规外泌体提取试剂进货价 2024-11-11
- 重庆正规外泌体提取试剂直销厂家 2024-11-11
- 厦门外泌体提取试剂平均价格 2024-11-11
- 芜湖外泌体提取试剂销售厂家 2024-11-10


- 开封RNA提取试剂推荐厂家 11-22
- 南昌RNA提取试剂报价 11-22
- 青岛RNA提取试剂生产厂家 11-22
- 昆明RNA提取试剂进货价 11-22
- 北京正规RNA提取试剂厂家批发价 11-22
- 厦门RNA提取试剂供应商 11-22
- 杭州RNA提取试剂哪里买 11-22
- 郑州正规RNA提取试剂生产厂家 11-22
- 温州RNA提取试剂产品介绍 11-22
- 石家庄RNA提取试剂厂家推荐 11-22