EAE动物模型的建立和应用为多发性硬化症(MS)的研究领域注入了新的活力,提供了丰富的实验数据和理论基础。通过精心设计和构建EAE动物模型,科学家们能够模拟MS在人体内的病理过程,从而深入探究疾病的发病机制、病理变化以及疗愈反应。这一模型的应用不仅为科学家们提供了大量可靠的实验数据,还帮助他们揭示了MS发病过程中的关键环节和分子机制。这些数据和理论基础为MS的深入研究奠定了坚实的基础,也为开发新的疗愈方法和药物提供了重要的参考依据。因此,EAE动物模型的建立和应用对于推动MS的研究进展具有不可替代的作用,为未来的科学研究和临床实践提供了新的方向和思路。与对照组相比,EAE模型组小鼠脊髓中活化的小胶质细胞数量增多。吉林大鼠eae模型动物实验外包
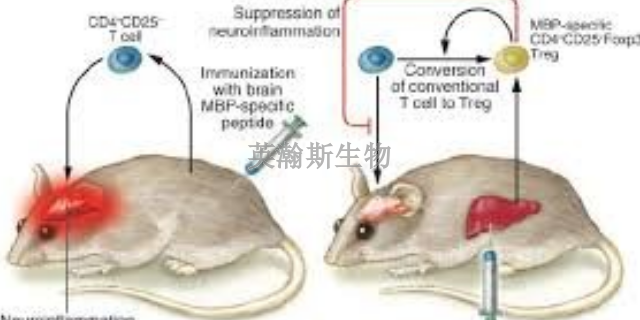
MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突胶质细胞糖蛋白,髓鞘的一种微量成分,属于免疫球蛋白超家族成员之一。t也是特定表达于***系统(CNS)的自身抗原,诱导多发性硬化症的原发性脱鞘特征。MOG(35-55)是髓鞘少突胶质细胞糖蛋白的免疫优势表位,能够诱导强烈的T细胞和B细胞应激反应,具高度致脑炎性,能够诱导啮齿类动物的实验性白身免疫性脑脊髓炎(EAE)模型。EAE是**普遍的MS动物模型,具有MS许多的临床和病理生理学特征。单次注射MOG(35-55)能够产生一种复发-缓解型神经性疾病,表现出大量斑块状脱髓鞘病症。1-甲基-4-苯基-1,.2,3,6-四氢吡啶(MPTP)诱导的多巴胺神经元损伤模型,免疫接种MOG(35-55)能抑制该神经元的白发再生功能。大鼠eae模型是哪家EAE小鼠模型如何制备?
临床医生和科学家使用各种工具来研究罕见病。 收集患者的数据和标本对于了解 TM 和 NMO 至关重要,但为了了解疾病的基本生物学特性,科学家通常使用疾病的动物模型。 迄今为止,还没有公认的特发性横贯性脊髓炎 (TM) 或视神经脊髓炎 (NMO) 动物模型。 然而,几十年来,一直存在一种称为实验性自身免疫性脑脊髓炎 (EAE) 的多发性硬化症实验模型。 该模型不完善,不能完全复制 MS,但可用于各种实验。 在人类中,MS、TM 和 NMO 被认为是由意外针对大脑、视神经或脊髓的免疫系统引起的。 在 EAE 中,小鼠的免疫系统准备好瞄准大脑、视神经或脊髓。 在人类中,免疫系统的不同部分(例如 B 细胞和 T 细胞)在 MS、TM 和 NMO 的发病机制中起着关键但可变的作用。
实验性自身免疫性脑脊髓炎(EAE)是一种以特异性致敏的CD4+T细胞介导为主的,以***系统内小血管周围出现单个核细胞浸润及髓鞘脱失为特征的自身免疫性疾病,是人类多发性硬化(MS)的理想动物模型,在临床神经免疫学的研究中具有重要意义。抗原佐剂为非特异性免疫增强剂,它可改变抗原的物理性状,延长抗原在体内的储留时间,刺激抗原提呈细胞及淋巴细胞,从而增强和扩大免疫应答效果,它还能引起迟发性血脑屏障通透性增加和自身免疫反应。EAE模型组小鼠脊髓中均出现髓鞘结构松散,密度降低等髓鞘脱失情况。
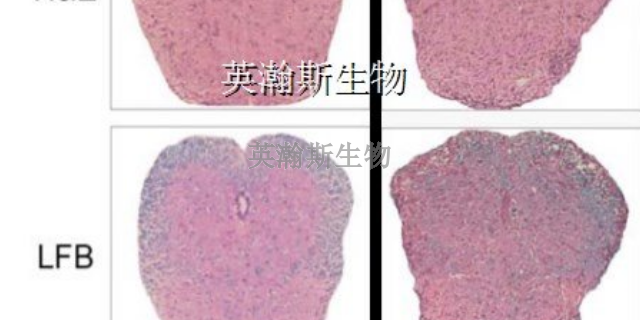
EAE是由针对CNS髓鞘发生免疫攻击的CD4+T介导的自身免疫性疾病,抗原致敏的T细胞穿过血脑屏障进入中枢,诱发对自身髓鞘抗原的免疫应答,导致脑及脊髓的免疫损伤。EAE是人类MS的经典动物模型,通过对EAE发病机制、病情发***展规律、临床及病理改变、***及预防等方面的深入研究,能够为MS的***提供充分的实验依据。国内外学者试用多种易感动物建立EAE模型,以期阐明MS及EAE的发病机制,并为其病情的监测、复发的预防、***方案的选择以及新疗法或新药物的筛选等提供可靠依据。自身免疫性脑脊髓(EAE)模型是古老、常用的人类MS实验模型。陕西真实的eae模型有哪家
只有EAE的NHP模型才可以对人源性抗体进行临床前评估。吉林大鼠eae模型动物实验外包
比较不同的神经功能损伤评分标准对小鼠实验性自身免疫性脑脊髓炎(EAE)运动功能障碍评估的效能。方法:应用MOG35-55多肽加完全福氏佐剂乳化后免疫20只C57BL/6小鼠,复制EAE小鼠模型,并使用3种不同的评分标准(Kono's5分法、Hooper's7分法、Weaver's15分法)观察和评估实验动物的发病情况,对实验小鼠在发病初期、高峰期的神经功能障碍进行定量的功能损伤评价。结果:3种评分标准比较,在发病初期,15分法和7分法评估神经损伤症状的敏感性相当,比5分法高;高峰期,以症状评分与病理评分的相关性程度来比较3种评分法的效度,15分法效度比较高,7分法次之。结论:Weaver's15分法评价EAE模型神经功能损伤症状,具有明显的优势,推荐作为今后EAE研究的优先评分法。吉林大鼠eae模型动物实验外包