EAE模型可以通过用髓磷脂抗原免疫小鼠来触发1. 抗原1 是什么能触发免疫系统产生抗体2 反对。 抗原1 在 EAE 中使用的靶向髓鞘蛋白包括髓鞘碱性蛋白 (MBP)、蛋白脂质蛋白 (PLP) 和髓鞘少突胶质细胞糖蛋白 (MOG)。 EAE 模型导致动物的大脑和脊髓脱髓鞘。 传统上,研究表明 T 辅助细胞3 是 EAE 的关键组成部分,但尚不清楚 B 细胞的作用在EAE模型。 在eae模型小鼠中,当受到刺激时,往往会*** T 细胞或 B 细胞,但通常不会同时强烈激发两者。该模型在大多数 (59%) 具有 B 细胞的小鼠中触发了 EAE4 和 T 细胞3 那是特定于 MOG 的。 EAE模型小鼠中致炎细胞Th17数量增加,抑炎细胞Treg和Breg数量降低。靠谱的eae模型动物实验外包
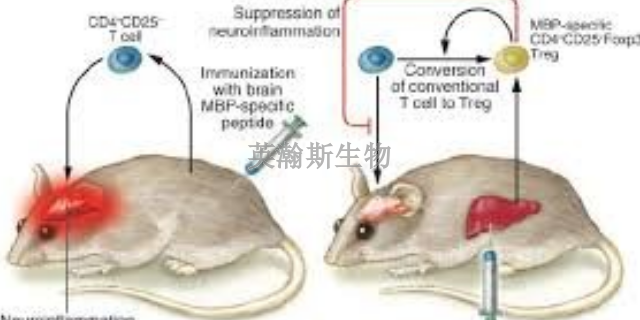
在EAE动物模型中,科学家们能够观察到一系列与多发性硬化症(MS)极为相似的炎症和神经损伤过程。这些过程不仅包括免疫细胞的浸润和激发,还涉及神经纤维的脱髓鞘病变以及神经元的损伤和死亡。通过观察EAE动物模型中的这些病理变化,科学家们能够更加直观地了解MS在人体内的发生机制,从而更加深入地探索疾病的本质。同时,这些观察结果也为科学家们提供了研究MS的新思路和新方向,有助于推动MS的疗愈和研究不断取得新的进展。因此,EAE动物模型在揭示MS病理过程方面发挥着重要作用,为科学家们深入研究这一复杂疾病提供了有力的工具。湖南推荐的eae模型造模方法继发性进展型EAE模型,伴有明显的脱髓鞘、神经胶质细胞活化。
EAE动物模型的研究不仅为我们深入探索多发性硬化症(MS)的发病机制提供了有力的工具,更在推动MS的临床诊断和***技术方面发挥着举足轻重的作用。通过对这一模型的深入研究,科学家们得以更***地了解MS的病理生理过程,从而为开发新的诊断方法提供了理论依据。同时,EAE动物模型也为评估新型***药物的疗效和安全性提供了重要的实验平台,为MS的临床***提供了更为精细和个性化的方案。此外,随着对EAE动物模型研究的不断深入,我们有望在未来发现更多针对MS的有效***方法,为患者带来更好的***效果和生活质量。因此,EAE动物模型的研究无疑将为MS的临床诊断和***技术的进步注入新的动力。
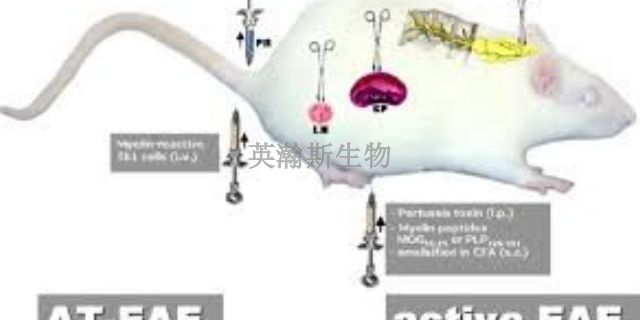
EAE模型的被动转移实验是研究其发病机制的**直接证据,也是研究EAE的***及预防措施的良好模型。将抗原***的PLP特异性T细胞转输给同一品系的正常大鼠或小鼠,也可引起EAE。MBP特异性自身反应性T细胞在MS的发病机制中也起着关键作用,T细胞必须先在外周活化,通过血管内皮细胞进入CNS才能致病。EAE的神经症状通常根据Kono等提出的标准分为5级。0级:无任何临床症状;1级:动物尾巴无力,2级:尾部无力+肢体无力,3级:肢体轻度麻痹,4级:肢体严重麻痹,被动翻身后不能复原;5级:濒死状态或死亡。EAE模型的诱导有主动诱导法和被动诱导法两种。
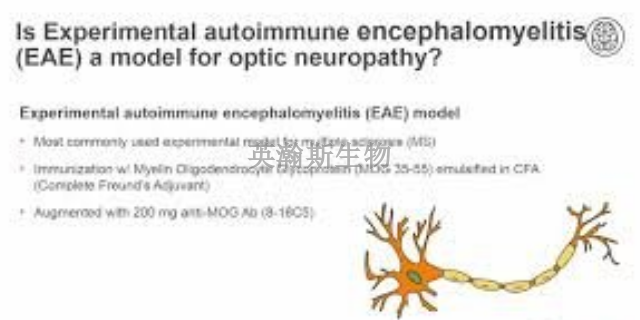
MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突胶质细胞糖蛋白,髓鞘的一种微量成分,属于免疫球蛋白超家族成员之一。t也是特定表达于***系统(CNS)的自身抗原,诱导多发性硬化症的原发性脱鞘特征。MOG(35-55)是髓鞘少突胶质细胞糖蛋白的免疫优势表位,能够诱导强烈的T细胞和B细胞应激反应,具高度致脑炎性,能够诱导啮齿类动物的实验性白身免疫性脑脊髓炎(EAE)模型。EAE是**普遍的MS动物模型,具有MS许多的临床和病理生理学特征。单次注射MOG(35-55)能够产生一种复发-缓解型神经性疾病,表现出大量斑块状脱髓鞘病症。1-甲基-4-苯基-1,.2,3,6-四氢吡啶(MPTP)诱导的多巴胺神经元损伤模型,免疫接种MOG(35-55)能抑制该神经元的白发再生功能。将抗原与佐剂的混合乳剂直接注射至动物体内,经过一定时间的潜伏期,诱导EAE模型的产生。重庆真实的eae模型实验外包
EAE模型的发生也存在动物性别差异。靠谱的eae模型动物实验外包
内分泌系统在EAE模型中的作用,以提供专业的观点并更好地理解EAE各种模型中内分泌与免疫系统之间的相互作用,从而为进一步详细研究奠定基础通过考虑和比较先前研究中使用的结果和模型来确定该领域。这导致在EAE模型中特定特殊的作用上存在矛盾的结果理解EAE各种模型中内分泌与免疫系统之间的相互作用,从而为进一步详细研究奠定基础通过考虑和比较先前研究中使用的结果和模型来确定该领域。EAE模型中特定***的作用产生矛盾的结果。靠谱的eae模型动物实验外包